Un antidépresseur bien connu pourrait-il prévenir les formes sévères de COVID-19 ?
Dans un contexte d’émergence de nouveaux variants du SARS-CoV-2, de plus en plus résistants aux vaccins et aux traitements, la recherche d’approches thérapeutiques complémentaires occupe une place importante. Des études in vitro et observationnelles ont récemment montré que la fluoxétine, connue pour ses propriétés antidépressives, atténue les signes cliniques de la COVID-19. Une recherche portée pour partie par des scientifiques de l’Institut de pharmacologie et de biologie structurale1 , publiée dans la revue International Journal of Molecular Sciences, confirme aujourd’hui un effet antiviral et anti-inflammatoire de la fluoxétine dans le modèle préclinique souris de la COVID-19.
Les filaments d'actine apparaissent en bleu, les cils en rouge et le virus en vert.
© Céline Cougoule
Cette recherche fait suite à de larges études observationnelles dont les résultats suggèrent une association significative entre la prise de fluoxétine et un moindre risque de décès chez des patients adultes hospitalisés pour une forme sévère de COVID-19. Elle renforce également les données obtenues in vitro qui démontrent que la modulation des voies des céramides (un type de lipide contenu dans la paroi des cellules) piégerait les récepteurs ACE-2 du virus à la surface des cellules, freinant ainsi son entrée dans les cellules cibles et sa capacité à se répliquer.
Dans cet article, les scientifiques montrent que l’administration thérapeutique post-infection de fluoxétine à une posologie modulant la voie des céramides réduit de plus de 90% la charge virale dans les poumons des souris traitées au deuxième jour post-infection, comparativement aux souris traitées par solution saline seule. De surcroît, cette substance active atténue les signes cliniques de la maladie et réduit fortement les taux de plusieurs marqueurs inflammatoires. Enfin, la fluoxétine montre une activité antivirale in vitro contre différents variants du SARS-CoV-2, y compris le variant Omicron BA.5.
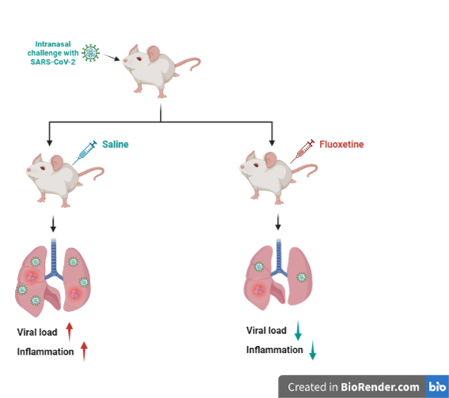
Ce modèle préclinique animal vient corroborer les données in vitro, observationnelles et d’essais cliniques qui suggèrent que les médicaments modulant les voies des céramides – et notamment les deux traitements « antidépresseurs » fluoxétine et fluvoxamine – ont un effet anti-SARS-CoV-2, probablement associé à un effet anti-inflammatoire. Ces résultats sont d’autant plus prometteurs que de précédents travaux suggèrent que ces antidépresseurs permettent de moduler les voies des céramides à une posologie standard chez l’humain. En effet, la fluvoxamine a déjà fait l’objet de plusieurs essais cliniques contrôlés randomisés et études de cohorte montrant un bénéfice clinique significatif dans la COVID-19 lorsque le traitement est prescrit à 200-300 mg/j, en ambulatoire ou en réanimation. Une absence d’effet est observée à une posologie plus faible (100 mg/j) chez des patients présentant un surpoids ou une obésité.
Ces résultats nécessitent d’être confirmés par des essais cliniques randomisés comparatifs. De larges essais cliniques internationaux testent actuellement l’efficacité de la fluvoxamine et de la fluoxétine – parmi lesquels l’essai AntiCoV coordonné par le DNDi – et sont, par conséquent, très attendus. S’ils sont positifs, ils ouvriront la voie à une approche thérapeutique novatrice, efficace, bien tolérée et à faible coût pour lutter contre la COVID-19, notamment dans les pays à ressources limitées.
- 1IPBS – CNRS / UT3
Bibliographie
Antiviral and anti-inflammatory activities of Fluoxetine in a SARS-CoV-2 infection mouse model.
David Péricat, Stephen Adonai Leon Icaza, Marina Sanchez Rico, Christiane Mühle, Iulia Zoicas, Fabian Schumacher, Rémi Planès, Raoul Mazar, Germain Gros1, Alexander Carpinteiro, Katrin Anne Becker, Jacques Izopet, Nathalie Strub-Wourgaft, Peter Sjö, Olivier Neyrolles, Burkhard Kleuser, Frédéric Li-mosin, Erich Gulbins, Johannes Kornhuber, Etienne Meunier, Nicolas Hoertel and Céline Cougoule.
Int. J. Mol. Sci. 2022, 23, 13623. https://www.mdpi.com/1422-0067/23/21/13623